李政忠副研究員參加2023國外參加研討會海報張貼
標題:2023國外參加研討會海報張貼
日期:2023/11/22~11/25, 地點: 泰國曼谷
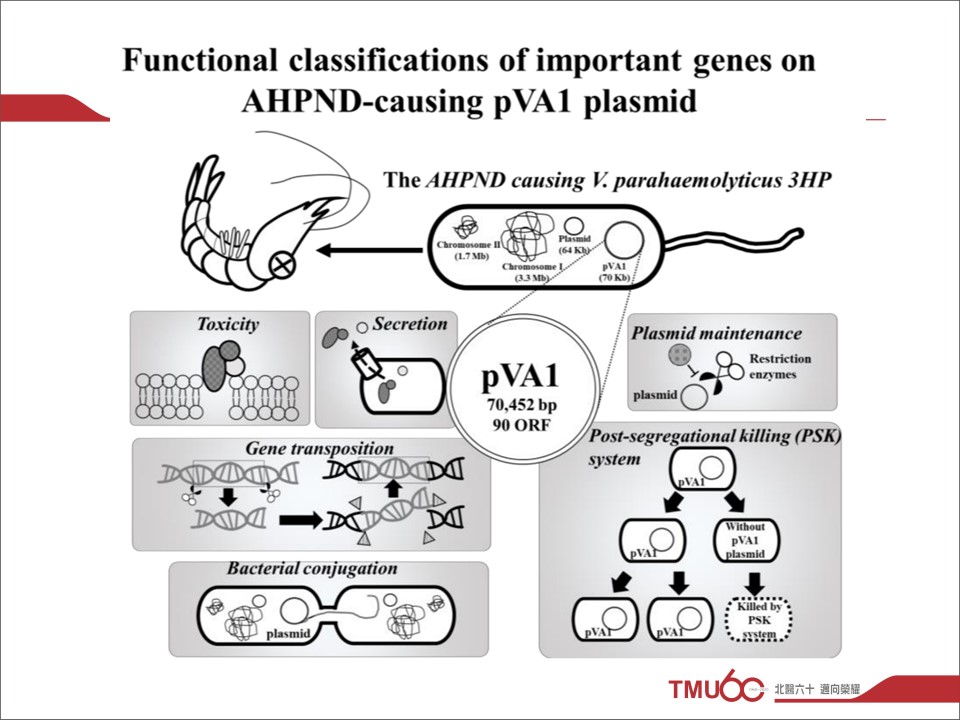
摘要:The 30th FAOBMB & 8th BMB Conference, 研究成果海報張貼
 3
3
標題:2023國外參加研討會海報張貼
日期:2023/11/22~11/25, 地點: 泰國曼谷
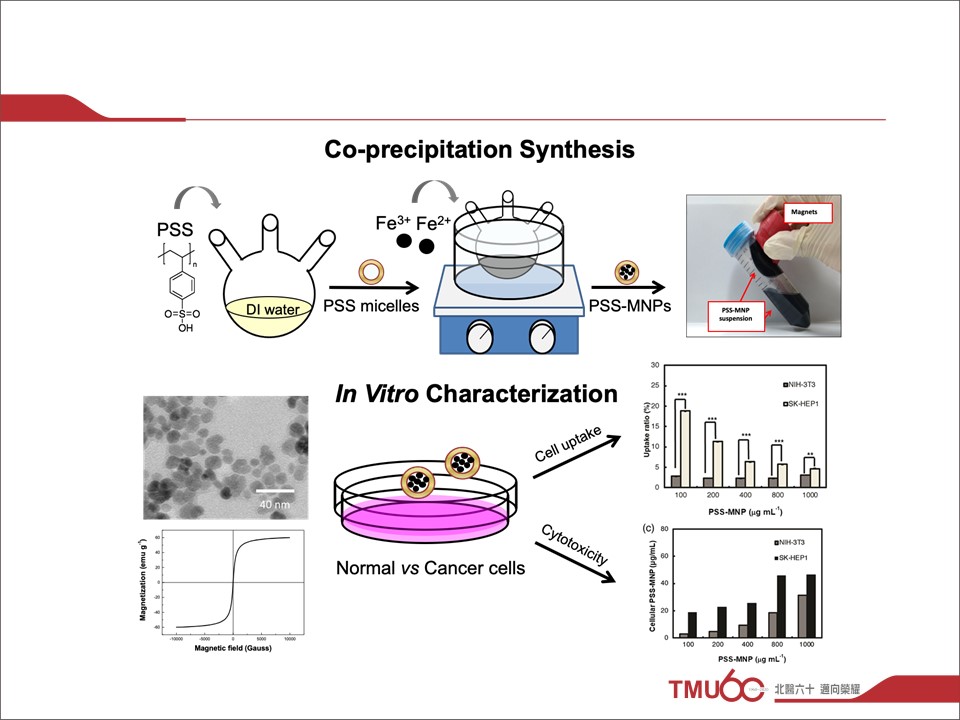
摘要:The 30th FAOBMB & 8th BMB Conference, 研究成果海報張貼
 3
3
標題:The Reacta Forum2023 regional Asian clinical trial annual forum
日期:2023/11/16-17
摘要:國際轉譯科學博士學位學程宋賢穎教授與日本千葉大學亞洲區域臨床試驗聯盟的主席團會議



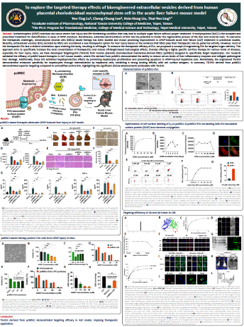
Think about the last time you reached out to grab a coffee cup or walked to the door. These everyday actions are powered by motor neurons and skeletal muscles, called the neuromuscular system. However, these simple actions can be a struggle for people with neuromuscular diseases (NMDs). The pathological mechanisms underlying most NMDs remain poorly understood, partly due to the lack of in vitro models that can comprehensively recapitulate multistage intercellular interactions and the physiological function of the motor unit (a motor neuron and muscle fibers it innervates).
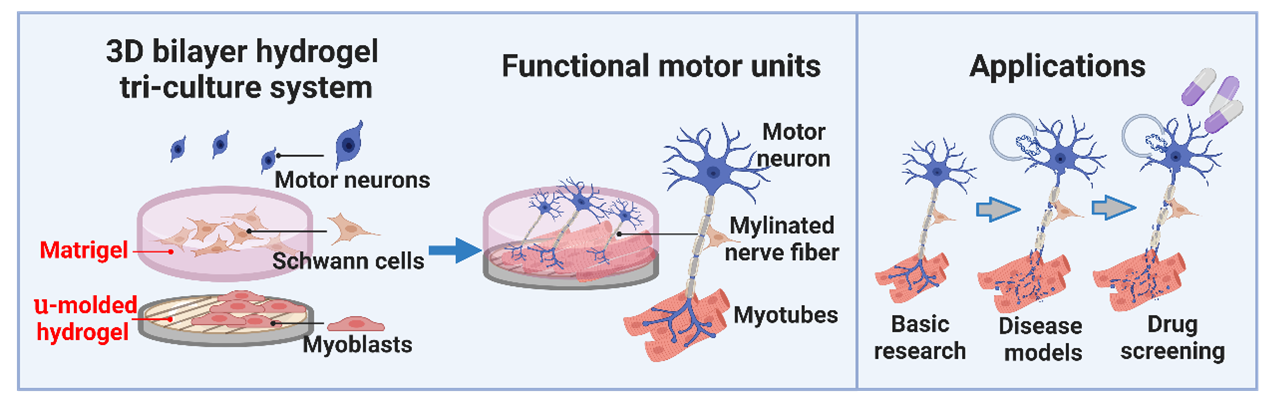
Professor Yu-Lung Lin from Taipei Medical University has recently published their work in Cell & Bioscience. He innovatively designed a three-dimensional bilayer hydrogel tri-culture system, which can accurately reproduce the structure and function of motor units in vitro, by sequentially co-culturing and differentiating myoblasts, Schwann cells, and motor neurons on two specific hydrogel substrates. This system has promoted the orderly arrangement of muscle fibers, the formation of myelin sheaths, and the establishment of functional neuromuscular junctions (NMJs).
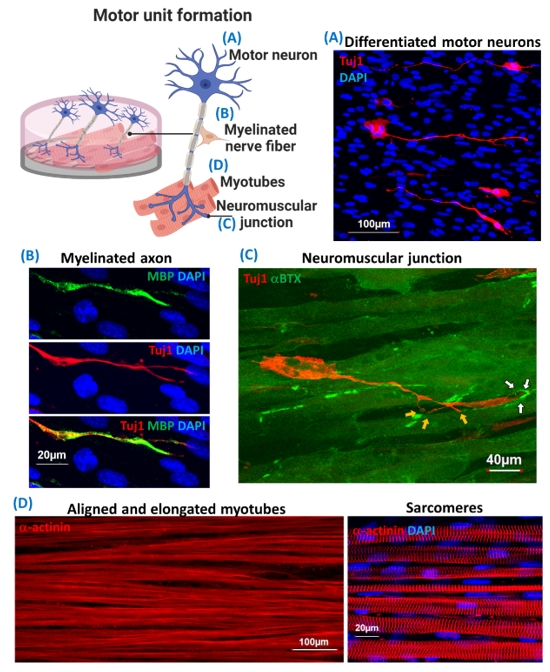
The importance of this research lies in providing a new perspective and tool for the study of NMDs. The tri-culture system can be used to investigate the basic biology of motor units and explore the pathologic mechanisms of NMDs, aiding in developing new therapeutic strategies. Moreover, because this model can reproduce MUs quickly and effectively without complex equipment, it opens up possibilities for applications such as disease modeling and drug screening, greatly enhancing research efficiency and feasibility.
Professor Lin’s research has opened new pathways for developing treatments for neuromuscular diseases. Establishing this model not only helps scientists better understand the disease’s progression but can also be used to test the effects of new drugs or treatment methods on neuromuscular units. Additionally, the high customizability of this model offers new possibilities for personalized medicine, with the potential to play a significant role in the fields of precision medicine and regenerative medicine in the future.
時間:2023.11.03~04
標題:2023發育生物學幹細胞與再生醫學國際研討會海報張貼(成功大學/臺灣大學/國際交流)



篇名:
Ribonucleotide reductase M2B in the myofibers modulates stem cell fate in skeletal muscle
探討在肌肉細胞中Ribonucleotide reductase M2B調節幹細胞分化命運的作用
論文介紹:
長久以來,科學家們不僅是追求使人類延年益壽的秘方,更是致力於讓人類在外觀或是身體機能各方面都長盛不衰。保持理想的生活品質對於老年人來說尤其重要,隨著年紀增加,骨骼肌質量和力量的衰退會導致行動及生活上的不便,因此維持骨骼肌的健康至關重要。
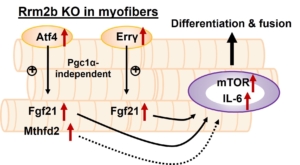
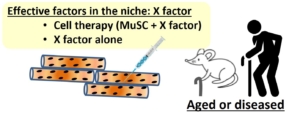
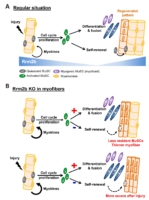
台北醫學大學陳怡帆副教授和閻雲教授在2022年7月29日刊登在《Nature》旗下的電子期刊《npj Regenerative Medicine》,其影響指數(Impact Factor)14.404,在細胞與組織工程領域排名全球第二,發表了他們最新的研究成果。文章中詳細闡述了有關核糖核苷酸還原酶 M2B (Rrm2b) 如何調節骨骼肌中的肌肉幹細胞及幹細胞面臨肌肉損傷的反應。簡單來說,骨骼肌的恆定仰賴於肌肉幹細胞 (MuSCs) 與其週邊微環境 (niche) 之間的相互作用。透過基因剔除小鼠模型,研究團隊發現了 Rrm2b 在肌肉纖維(微環境的一部分)中特異性的缺失會造成小鼠肌肉質量和力量的喪失,這些 Rrm2b 肌纖維特異性剔除的小鼠,他們肌肉的再生能力也受到限制。此外,肌肉纖維中Rrm2b的缺乏也導致了線粒體相關的缺陷,使小鼠表現出粒線粒體肌病 (mitochondrial myopathy) 的部分特徵。
在另一方面,陳教授的團隊也與林依璿博士合作,透過RNA定序鑑定出幾種由 Rrm2b 缺失的肌肉纖維中釋放的肌肉激素 (myokine),包含 FGF-21、GDF-15 和 Mthfd2。這些肌肉激素會促使肌肉幹細胞不斷地分化,使幹細胞無法維持在靜止的狀態。肌肉幹細胞在分化及自我更新之間的失衡,使得肌肉幹細胞的總數減少,進而導致肌肉的病變及再生能力方面的缺失。
陳教授的研究成果確立了 Rrm2b 對於維持骨骼肌恆定中所扮演的角色。肌肉纖維中的 Rrm2b 於調節肌肉幹細胞的狀態發揮著關鍵作用,未來也有機會發展出治療肌肉相關疾病的策略,Rrm2b 基因剔除小鼠模型也有可能作為研究哺乳動物線粒體肌病的疾病模型。憑藉這些驚人的研究結果,期望未來能將這些研究成果推展至臨床應用,促進肌肉健康,提升老年人的生活品質。